传统上认为,成年人的神经元数量固定,不会新增。然而,在原有神经元上刷新记忆之余,在需要的时候为新的记忆补充新的神经元是最为直接有效的局部和网络重构方式。越来越多新的证据支持大脑会增加新的用于记忆的神经元,而不只是优化更新原有神经元的突触连接、增加新的搜索索引(哈希)。
在储存食物过冬的鸟类中,由于神经生成(neurogenesis),海马体的大小在每年秋冬季都会增大[1]。成年大鼠脑中的脑室下区(subventricular zone,SVZ)会产生嗅觉神经元;在大鼠发育早期,脑室下区更是神经元的重要来源[2]。
目前成年人大脑中可能仍有新增神经元的区域包括脑室下区、海马和纹状体(striatum) [3]。小鼠脑室下区的胆碱能神经元((释放乙酰胆碱、)表达乙酰胆碱酯酶以终止突触传递,choline acetyltransferase–positive (ChAT(+)) neurons)被前扣带回(ACC)的神经元激活后,脑室下区中原本处于静息状态的神经干细胞被激活、分化生长[4]。
海马齿状回(上一章节介绍的dentate gyrus, DG)在小鼠一生中逐渐增加新神经元,但随着年龄增大,新增神经元的数量减少[5],这样老年个体已有的记忆变成了版本更加固定的数据库。
育龄女性血液中孕酮水平在孕期和月经来潮前较高。月经周期中孕酮水平与海马CA2/CA3区域(CA2与CA3分割困难)的体积正相关,而与内嗅皮层的体积负相关(我们在本书空间探索的章节会着重介绍内嗅皮层,Entorhinal cortex)。这些区域中的雌激素和孕酮受体表达水平比大脑其他部分更高[6]。
大脑特定区域的体积变化,表明细胞数目、体积或细胞外其他体积的变化。图5.2讲到,人类大脑灰质体积平均在5.9岁达到峰值,而白质体积在28.7岁达到峰值。对人类成年阶段神经生成的研究更困难,且一直存在争议[7-10]。当前神经科学对神经生成的研究多基于小鼠,而小鼠中发生神经生成的区域--“齿状回”可能不是人类海马体新神经元形成的主要部位。
调节细胞骨架微管稳定性的双皮质素(doublecortin,DCX)表达是研究神经元前体细胞(neuroblasts,即神经干细胞)的常用标志物。在成年的猪、猴和人的海马 CA1-CA4区的许多细胞中都检测到了DCX表达,说明有新生的神经元[11]。这些动物中新生神经元的类型和主要出现部位与小鼠大鼠不尽相同,例如在猪、猴子和人类的海马CA1-CA4区域中新产生的除了齿状回颗粒细胞(granule cells),还有很多中间神经元(结合前后文的一些章节,新增的不只是细节,还有涉及多个神经元的范式)。人类等新增的中间神经元可能涉及在小鼠中不存在的新类型[12]。
另一项对人脑细胞基因表达的研究在成年人大脑海马齿状回中检测到了神经干细胞,Ki67蛋白抗体结果还表明成年人的神经干细胞也有增殖[13]。以上证据间接支持了成年人大脑中存在神经生成,新增的神经元可能对应新的记忆。
另一项重要证据来自巧妙运用了冷战时期大量核试验残留在人群中的天然标记。根据放射性碳定年法的研究,在一个中年人的海马体中,每天大约有700个新生神经元,每年更新的神经元合计为海马体细胞总数的1.75% ,累计1/3的海马体神经元在一生中会被更新[14]。而未被更新的那部分神经元死亡虽慢,却没有替补。有更新的那1/3的神经元半衰期是7.1年,比不更新的那部分死亡速度快了10倍 。即使是“临时槽位”,这些新生神经元也可以存储一些新概念或事件,而不必过度腾挪,这样后续还可以慢慢整理、优化。
这与当前人工智能神经网络,自训练初始时起人工神经元数目就不变不同。新增神经元以应对新增的,截然不同的记忆。这相比调节已有的神经网络,所需的重置连接的成本可能更低。新增的神经元后续连接的多少还可以再定。
新增的神经细胞,不止是神经元,还包括小胶质细胞(microglia)。至少在发育过程中,小胶质细胞参与调控表达小清蛋白的中间神经元是否被整合进入以锥体神经元为主的神经回路[15](未有充分连接的新生中间神经元后续可能被清除)。颞叶内侧癫痫患者的神经元新生较少,而星形胶质细胞的生成不受影响[16]。
在衰老过程中(可能还有在其他炎症状态下) ,免疫细胞浸润脑室下区和齿状回。自然杀伤细胞会消除齿状回中老化的神经细胞,从而导致神经生成和认知功能随着年龄的增长而下降[17]。干细胞储备的急性动员,如中风后或巨大压力下,可能意味着其在长期的耗竭[18],也可能导致长期来看学习记忆能力的下降。
主要依据小鼠和大鼠的研究,海马齿状回新增的神经元在诞生后的几周内成熟并被整合到神经元回路中(图16.1),这些还没有发育完成的新神经元比成熟的神经元的细胞体更容易被激活[19,20,21]。由于新生神经元的出现与其整合到神经回路之间有2-3周的延迟(有些可能更长),笔者这些新生神经元以及等待与其连接的现有神经元需要在神经活动激活决定要新生神经元时即被标记,比如通过表观遗传学机制。
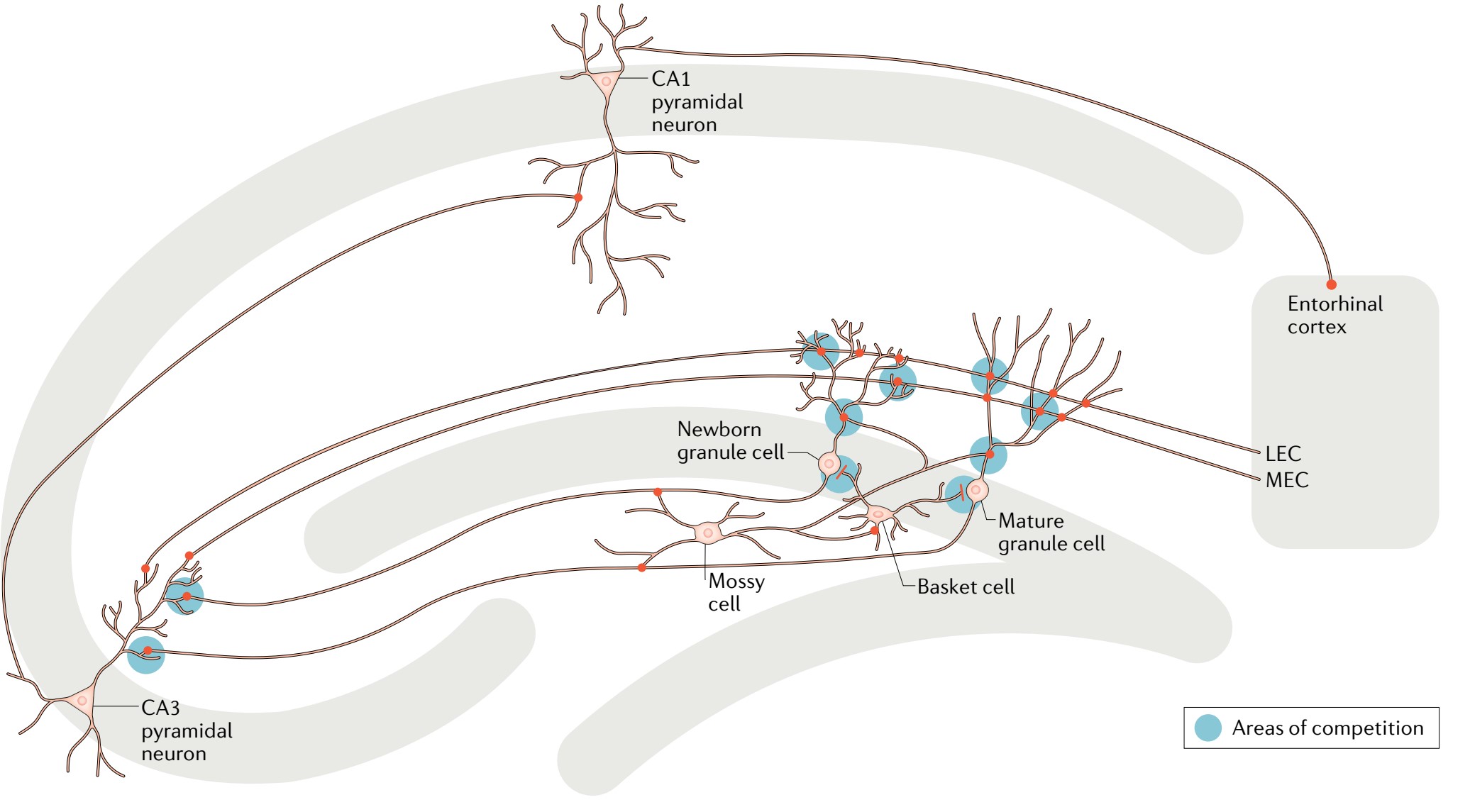
图16.1: 成年海马新生颗粒细胞的回路功能。齿状回(DG)中的新生颗粒细胞接收到的来自外侧内嗅皮层(LEC)的输入比来自内侧内嗅皮层(MEC)的输入更强。未成熟颗粒细胞也可以影响齿状回回路的活跃度,比如通过直接刺激成熟颗粒细胞,或更间接地通过激活抑制性中间神经元(如表达小清蛋白的篮状细胞)或激活位于齿状回内颗粒层的苔藓细胞(hilar mossy cells,也属于抑制性中间神经元)。随着成熟,颗粒细胞受到强烈的周围抑制,并在CA3锥体细胞上形成大的钮扣状结构,从而调节CA3区和CA1区的输出,信息从那里流回内嗅皮层和其他关联皮层。不同成熟阶段的新生神经元对DG回路的活动和信息流及其输出到CA3区的确切影响,需要通过体外和体内成像和电生理记录来进一步分析。蓝色阴影区域表示新的神经元可能不得不与已存在的细胞竞争突触前和突触后的神经元伙伴。
记忆形成的每一步,其成功概率并不是很高[21,22] ,这意味着需要更多的练习、情感或奖励(见强化学习的章节)来增加记忆形成的概率。这也意味着已切实记录在神经元及其突触中的事情不会随着我们年龄的增长而被灾难性地覆盖。虽然我们日常记起的往往是与某个人、事、地点索引最近的、或者印象最深的事件,那些神经元在本地计算时所忽略的事件,其对应的存储仍然存在,而且是可搜索的。这或可启发用于应对灾难性遗忘的机器学习算法和硬件。
新的树突棘向神经递质(例如谷氨酸盐)的来源处生长[23]。对小鼠的研究表明,齿状回新生的神经元会出现两波部分消失的现象——第一波在神经元生成后48小时内,第二波在神经元生成后12-16天[24]。第二波去除了还没有 NMDA 受体输入、没有被整合到现有神经回路中的新生神经元,而幸存的那些连接了CA3区11至15个锥体神经元(图16.1)[21]。这是一种“宽进严出”的精简机制,“学而时习之”的科学依据。至少有一项研究提示,猕猴中新生神经元的整合耗时更长、在6个月后仍在进行[22]。
上一章节与海马体位置一起介绍的内嗅皮层进一步分为LEC(lateral entorhinal cortex)和MEC(medial entorhinal cortex)。后者我们在空间探索、模式复用的章节详细讲,而LEC不仅为海马齿状回的颗粒细胞提供时间信息(本书后面章节),还对海马CA3的锥体神经元有精准调控[23]。
我们在第15节首次讲到海马体与大脑皮层之间的连接可能是一个持续优化迭代的哈希索引,而海马体内部不同区域在已有和未有的比较、已决定存储多少的过程中起作用。根据神经网络模拟,从内嗅皮层直接到海马 CA1(远离细胞体,例如胞体)的单突触通路能够支持统计学习(更新权重),属于对已有连接模式的调用、神经连接越使用越健壮 ; 而来自内鼻皮质、经过三个突触的通路,即通过齿状回和 CA3到 CA1(靠近细胞体顶端树突的突触侧枝[17.28] ,可通过单个事件学习[31.5],是更细节的记录。这样不同的通路在神经系统中很常见,可以确保快速反应,同时允许重要的新信息被记录下来,为未来做准备。
小结:在人类中,新神经元的增加,例如成年阶段的神经生成,最为人所知的发生在海马体齿状回。广为人知的经典记忆巩固模型认为,信息暂时存储在海马体中,并在几周内转移到大脑新皮层。与之相反,新出现的证据将我引向了一个更加基于硬件的模型,即内嗅-海马波和涟漪直接搜索大脑皮层中的现有信息,并且在任何与现有信息不匹配的地方,鼓励新信息以新的分支或新的神经元的形式存储,在其中海马锥体神经元充当哈希函数。
思考题:你认为我们每天如何分配数百个新增的海马体神经元?它们中有多少神经元能存活成成熟的形态?针对一个遥远的事件有多少海马和皮层神经元可以被留下?
参考文献:
[1] DF, Sherry, and Hoshooley JS. 2010. “Seasonal Hippocampal Plasticity in Food-Storing Birds.” Philosophical Transactions of the Royal Society of London. Series B, Biological Sciences 365 (1542): 933–43. https://doi.org/10.1098/RSTB.2009.0220.
[2] Rakic, Pasko. 2009. “Evolution of the Neocortex: A Perspective from Developmental Biology.” Nature Reviews. Neuroscience 10 (10): 724–735.
[3] Denoth-Lippuner, Annina, and Sebastian Jessberger. 2021. “Formation and Integration of New Neurons in the Adult Hippocampus.” Nature Reviews Neuroscience 22 (4): 223–36. doi.org/10.1038/s41583-021-00433-z.
[4] Naffaa, M. M., & Yin, H. H. (2024). A cholinergic signaling pathway underlying cortical circuit activation of quiescent neural stem cells in the lateral ventricle. Science Signaling, 17(855). doi.org/10.1126/scisignal.adk8810
[5] Kuhn, H G, H Dickinson-Anson, and F H Gage. 1996. “Neurogenesis in the Dentate Gyrus of the Adult Rat: Age-Related Decrease of Neuronal Progenitor Proliferation.” The Journal of Neuroscience : The Official Journal of the Society for Neuroscience 16 (6): 2027–2033.
[6] Taylor, C. M., Pritschet, L., Olsen, R. K., Layher, E., Santander, T., Grafton, S. T., & Jacobs, E. G. (2020). Progesterone shapes medial temporal lobe volume across the human menstrual cycle. NeuroImage, 220, 117126. https://doi.org/10.1016/j.neuroimage.2020.117125
[7] Denoth-Lippuner, Annina, and Sebastian Jessberger. 2021. “Formation and Integration of New Neurons in the Adult Hippocampus.” Nature Reviews Neuroscience 22 (4): 223–36. https://doi.org/10.1038/s41583-021-00433-z.
[8] Spalding, Kirsty L, Olaf Bergmann, Kanar Alkass, Samuel Bernard, Mehran Salehpour, Hagen B Huttner, Emil Boström, et al. 2013. “Dynamics of Hippocampal Neurogenesis in Adult Humans.” Cell 153 (6): 1219–27. https://doi.org/10.1016/j.cell.2013.05.002.
[9] Tobin, Matthew K., Kianna Musaraca, Ahmed Disouky, Aashutosh Shetti, Abdullah Bheri, William G. Honer, Namhee Kim, et al. 2019. “Human Hippocampal Neurogenesis Persists in Aged Adults and Alzheimer’s Disease Patients.” Cell Stem Cell 24 (6): 974-982.e3. https://doi.org/10.1016/J.STEM.2019.05.003.
[10] Jurkowski, Michal P, Luis Bettio, Emma K Woo, Anna Patten, Suk-Yu Yau, and Joana Gil-Mohapel. 2020. “Beyond the Hippocampus and the SVZ: Adult Neurogenesis Throughout the Brain.” Frontiers in Cellular Neuroscience 14: 576444. https://doi.org/10.3389/fncel.2020.576444.
[11] Franjic, Daniel, Mario Skarica, Shaojie Ma, Jon I. Arellano, Andrew T.N. Tebbenkamp, Jinmyung Choi, Chuan Xu, et al. 2022. “Transcriptomic Taxonomy and Neurogenic Trajectories of Adult Human, Macaque, and Pig Hippocampal and Entorhinal Cells.” Neuron 110 (3): 452-469.e14. doi.org/10.1016/J.NEURON.2021.10.036.
[12] Krienen, Fenna M., Melissa Goldman, Qiangge Zhang, Ricardo C H Del Rosario, Marta Florio, Robert Machold, Arpiar Saunders, et al. 2020. “Innovations Present in the Primate Interneuron Repertoire.” Nature 586 (7828): 262–69. https://doi.org/10.1038/s41586-020-2781-z.
[13] Dumitru, I., Paterlini, M., Zamboni, M., Ziegenhain, C., Giatrellis, S., Saghaleyni, R., Björklund, Å., Alkass, K., Tata, M., Druid, H., Sandberg, R., & Frisén, J. (2025). Identification of proliferating neural progenitors in the adult human hippocampus. Science, 389(6755), 58–63. https://doi.org/10.1126/science.adu9575
[14] Spalding, Kirsty L, Olaf Bergmann, Kanar Alkass, Samuel Bernard, Mehran Salehpour, Hagen B Huttner, Emil Boström, et al. 2013. “Dynamics of Hippocampal Neurogenesis in Adult Humans.” Cell 153 (6): 1219–27. https://doi.org/10.1016/j.cell.2013.05.002.
[15] Cossart, Rosa, and Sonia Garel. 2022. “Step by Step: Cells with Multiple Functions in Cortical Circuit Assembly.” Nature Reviews Neuroscience 23 (7): 395–410. https://doi.org/10.1038/s41583-022-00585-6.
[16] Ammothumkandy, Aswathy, Kristine Ravina, Victoria Wolseley, Alexandria N. Tartt, Pen-Ning Yu, Luis Corona, Naibo Zhang, et al. 2022. “Altered Adult Neurogenesis and Gliogenesis in Patients with Mesial Temporal Lobe Epilepsy.” Nature Neuroscience 25 (4): 493–503. https://doi.org/10.1038/s41593-022-01044-2.
[17]
[18] Urbán, Noelia, Isabelle Maria Blomfield, and François Guillemot. 2019. “Quiescence of Adult Mammalian Neural Stem Cells: A Highly Regulated Rest.” Neuron 104 (5): 834–848.
[19] Danielson, Nathan B, Patrick Kaifosh, Jeffrey D Zaremba, Matthew Lovett-Barron, Joseph Tsai, Christine A Denny, Elizabeth M Balough, et al. 2016. “Distinct Contribution of Adult-Born Hippocampal Granule Cells to Context Encoding.” Neuron 90 (1): 101–12. https://doi.org/10.1016/j.neuron.2016.02.019.
[20] Klinzing, Jens G., Niels Niethard, and Jan Born. 2019. “Mechanisms of Systems Memory Consolidation during Sleep.” Nature Neuroscience 22 (10): 1598–1610. https://doi.org/10.1038/s41593-019-0467-3.
[21] Denoth-Lippuner, Annina, and Sebastian Jessberger. 2021. “Formation and Integration of New Neurons in the Adult Hippocampus.” Nature Reviews Neuroscience 22 (4): 223–236.
[22] Kohler, S. J., Williams, N. I., Stanton, G. B., Cameron, J. L. & Greenough, W. T. Maturation time of new granule cells in the dentate gyrus of adult macaque monkeys exceeds six months. Proc. Natl. Acad. Sci. U. S. A. 108, 10326–10331 (2011).
[23] De La Torre RG, Zemelman BV, Clopath C, BasuJ.Science. 2025 Dec 11;390(6778):eadn0623. doi: 10.1126/science.adn0623. Epub 2025 Dec 11.PMID: 41166439
[22] Branco, Tiago, and Kevin Staras. 2009. “The Probability of Neurotransmitter Release: Variability and Feedback Control at Single Synapses.” Nature Reviews. Neuroscience 10 (5): 373–383.
[23] Nägerl, U Valentin, German Köstinger, John C Anderson, Kevan A C Martin, and Tobias Bonhoeffer. 2007. “Protracted Synaptogenesis after Activity-Dependent Spinogenesis in Hippocampal Neurons.” The Journal of Neuroscience : The Official Journal of the Society for Neuroscience 27 (30): 8149–8156.
[24] Li, Ya-Dong, Yan-Jia Luo, Ze-Ka Chen, Luis Quintanilla, Yoan Cherasse, Libo Zhang, Michael Lazarus, Zhi-Li Huang, and Juan Song. 2022. “Hypothalamic Modulation of Adult Hippocampal Neurogenesis in Mice Confers Activity-Dependent Regulation of Memory and Anxiety-like Behavior.” Nature Neuroscience 25 (5): 630–645.
[28] Aksoy-Aksel, Ayla, and Denise Manahan-Vaughan. 2013. “The Temporoammonic Input to the Hippocampal CA1 Region Displays Distinctly Different Synaptic Plasticity Compared to the Schaffer Collateral Input in Vivo: Significance for Synaptic Information Processing.” Frontiers in Synaptic Neuroscience 5: 5. https://doi.org/10.3389/fnsyn.2013.00005.
[17.30] Akers, Katherine G, Alonso Martinez-Canabal, Leonardo Restivo, Adelaide P Yiu, Antonietta De Cristofaro, Hwa-Lin Liz Hsiang, Anne L Wheeler, et al. 2014. “Hippocampal Neurogenesis Regulates Forgetting During Adulthood and Infancy.” Science 344 (6184): 598–602. https://doi.org/10.1126/science.1248903.
[17.31] Franjic, Daniel, Mario Skarica, Shaojie Ma, Jon I. Arellano, Andrew T.N. Tebbenkamp, Jinmyung Choi, Chuan Xu, et al. 2022. “Transcriptomic Taxonomy and Neurogenic Trajectories of Adult Human, Macaque, and Pig Hippocampal and Entorhinal Cells.” Neuron 110 (3): 452-469.e14.
0
推荐




 京公网安备 11010502034662号
京公网安备 11010502034662号 