我们在本书第6节介绍了大部分神经元树突分枝上均匀排列的树突棘机构。记忆的物质基础不只到单个神经元细胞,树突经细胞体(细胞核周围)到轴突的整个形态结构,包括各树突棘(图17.1)的形态和朝向、其中的分子,都决定着该细胞对刺激的反应。我们在第6节也已经看到了根据树突棘形态计算的亿欧姆级电阻,可能使得大部分信号止于树突。
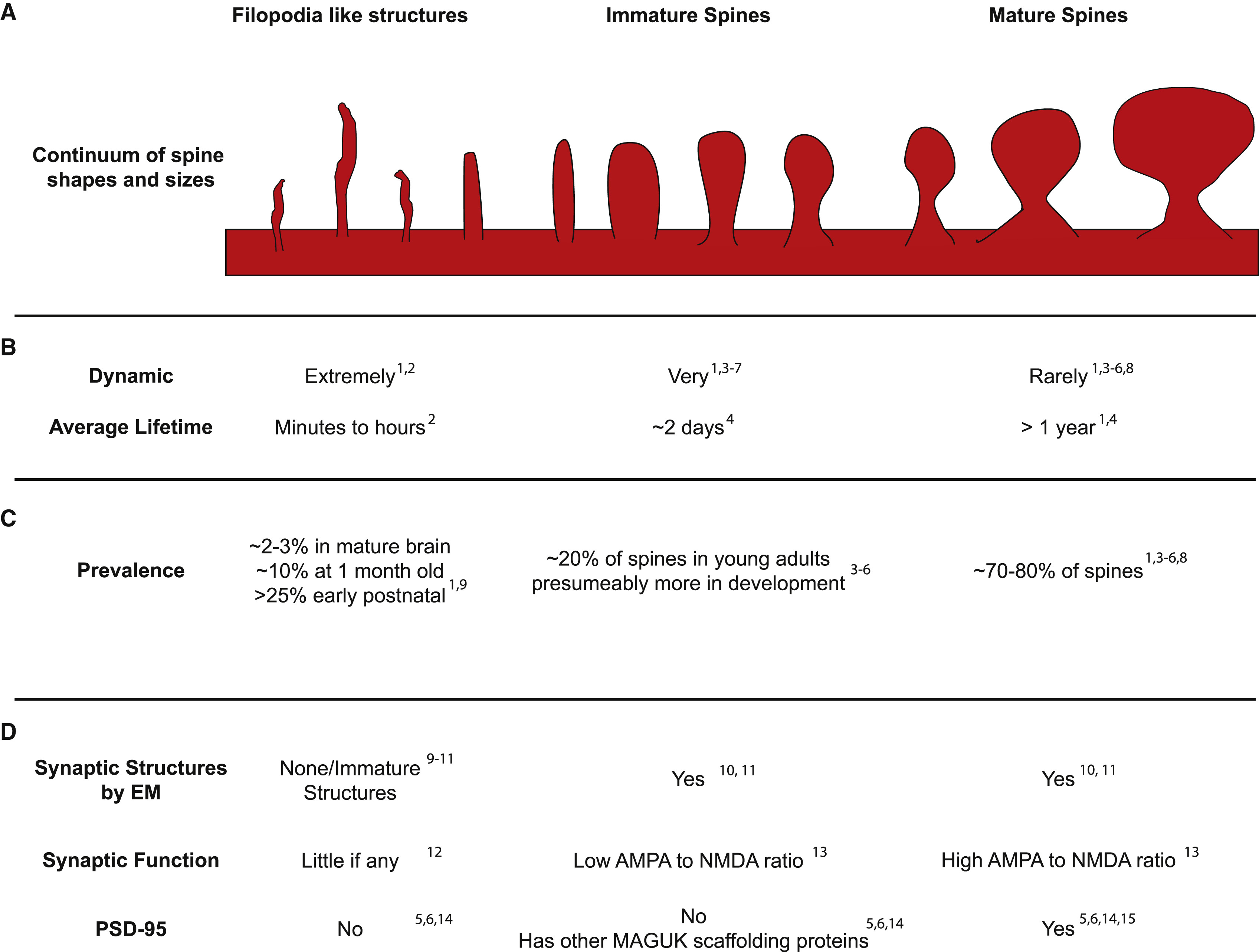
图17.1 根据形态由细到粗展示的丝状伪足、未成熟树突棘和成熟树突棘。仅根据尺寸对前两者的区分有难度。成年后成熟树突棘约占80%。来自[1]。
虽然发育早期预设的树突棘阵列可能都是细长的(例如1微米间距、1.7微米长),成年后突触之间权重有数量级差异,改变一两个大的突触就可能改变一个细胞整体表现,例如调整该神经元最敏感的光栅朝向[2];而其他突触存储的信息实际上还在,只是没有竞争优势。根据小鼠视觉皮层(V1)第2-3层区域锥体神经元统计的树突棘头部体积呈双log叠加的分布[3],即大部分树突棘可能仅获得了一次显著增大。这也是神经计算稀疏性的体现。海马体CA1的锥体神经元突触大小也呈二元分布[4]。
对大鼠大脑海马体切片的体外实验展现了树突棘“量子化”的单次显著增大(图17.2)[7]。在大脑中,这种树突棘体积的增大还需要核糖体(制造新蛋白,但也可以靠吸引已有蛋白)、受体蛋白、细胞骨架蛋白(actin、PSD-95等)等使其稳定。未成熟树突棘的颈部粗,会更快把接受的钙离子电流漏到树突轴,可能有更广泛的激活。而成熟树突棘较细的颈部更好地把钙离子留在原处、促进其自身庞大。
同样是接受谷氨酸神经递质后打开的钙离子通道,未成熟树突棘的NMDA受体(N-methyl-D-aspartate receptors)较多,倾向于赫布学习(同时激活的倾向于连接,是一种关联),而成熟树突棘的AMPA受体(α-amino-3-hydroxy-5-methyl-4- isoxazole propionic acid receptors)较多(图17.1),倾向于反赫布学习(强调区别)。
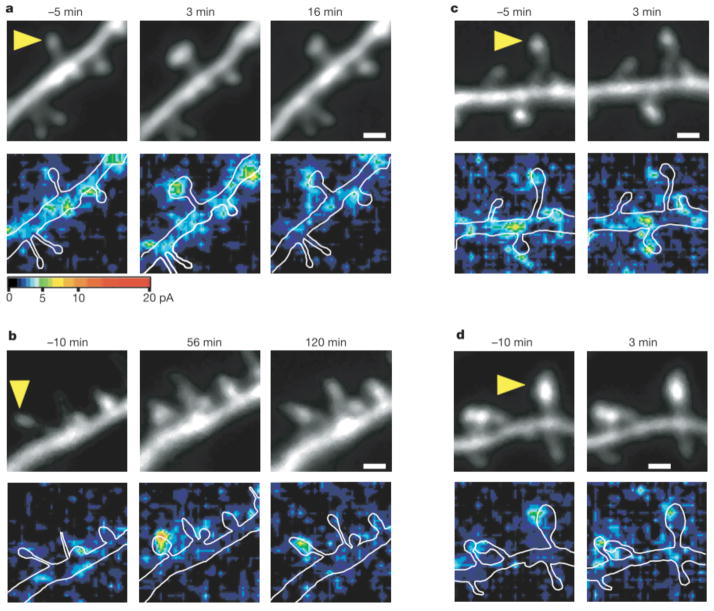
图17.2 大鼠海马体切片定点释放谷氨酸导致树突棘头部的扩大(a-d上图)的和AMPA受体介导的电流的增强(a-d下图)。箭头标注的较细树突棘从定点释放前(-5或-10分钟)与释放后比较。
因此,树突棘在时间上的稳定性大致与头部大小呈正比(图17.3)[1,8]。
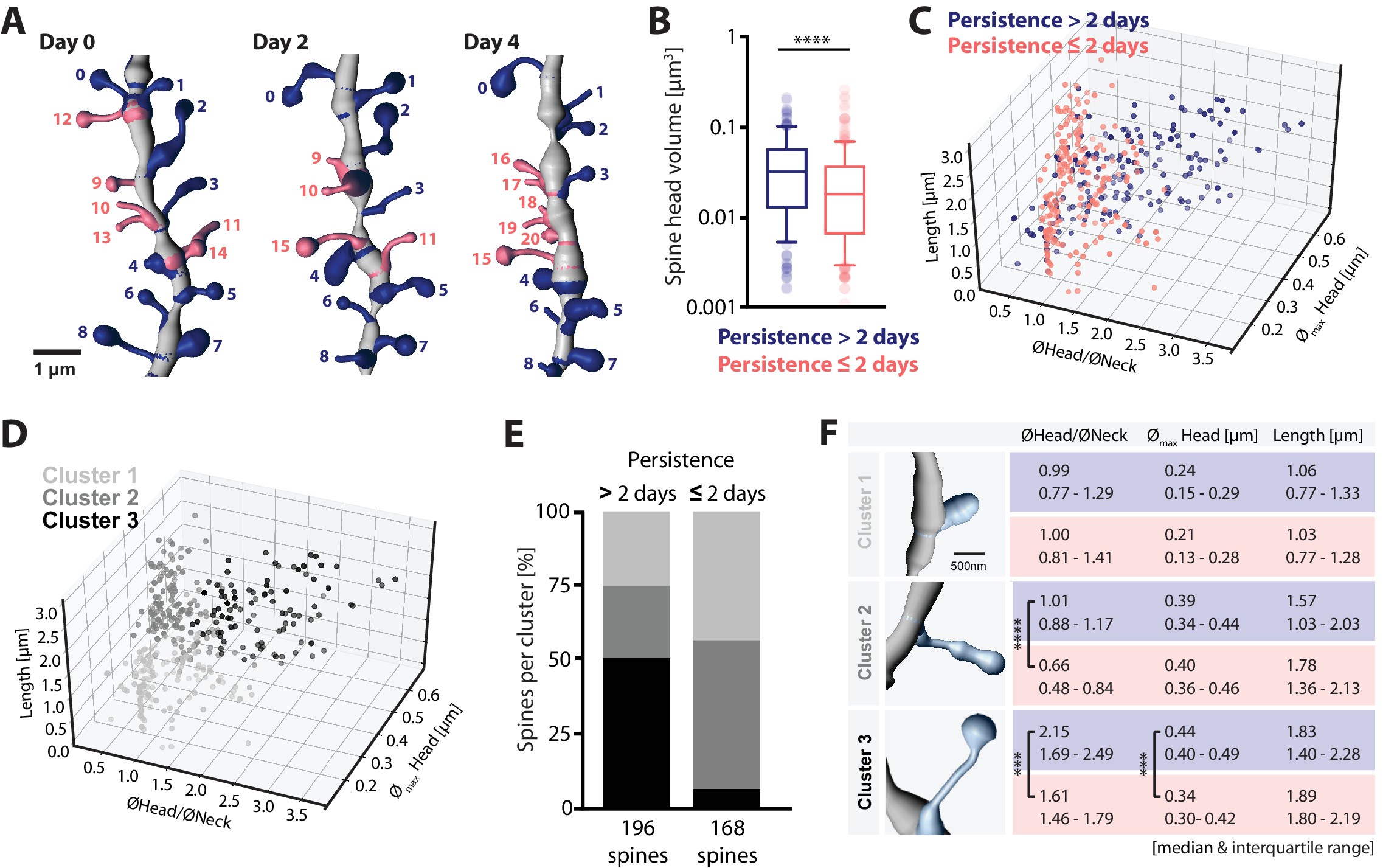
图17.3 小鼠海马体树突棘在几天内的存续与初始头部体积、头部、颈部尺寸的关系。超分辨率显微镜(2P-STED)结果。来自[8]
虽然大部分突触是单个轴突对树突棘的输入,还可以看到一些两个以上输入的情况(图17.4、图17.5)[9,10],可以都在树突棘头部,也有些涉及颈部或者侧面的,预计都属于本地计算。我们在本书第5节、第7节介绍的中间神经元如果在细胞体而不是树突棘上施加抑制(图17.5),则会有更大的突触扣结(bouton),以保证信号强度。一项尚有争议的研究认为,串珠样的结构才是轴突的常态[11],可能有助于电信号的保真和传播速度;小鼠大脑皮层轴突上的突触间距约5微米[12],也是一重阵列。
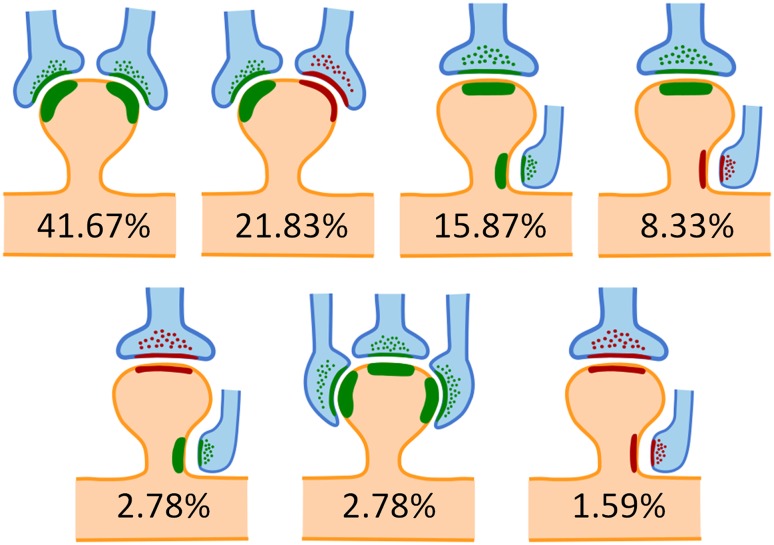
图17.4 未成年大鼠感觉皮层各层统计归纳的树突棘接受多个输入的情形。观察的4558个树突棘中5.57% (254个) 有2-3个突触,各自占比如图所示,红色为兴奋性突触、绿色为抑制性突触。还有约5%的更稀有的组合没有画出。来自[9]
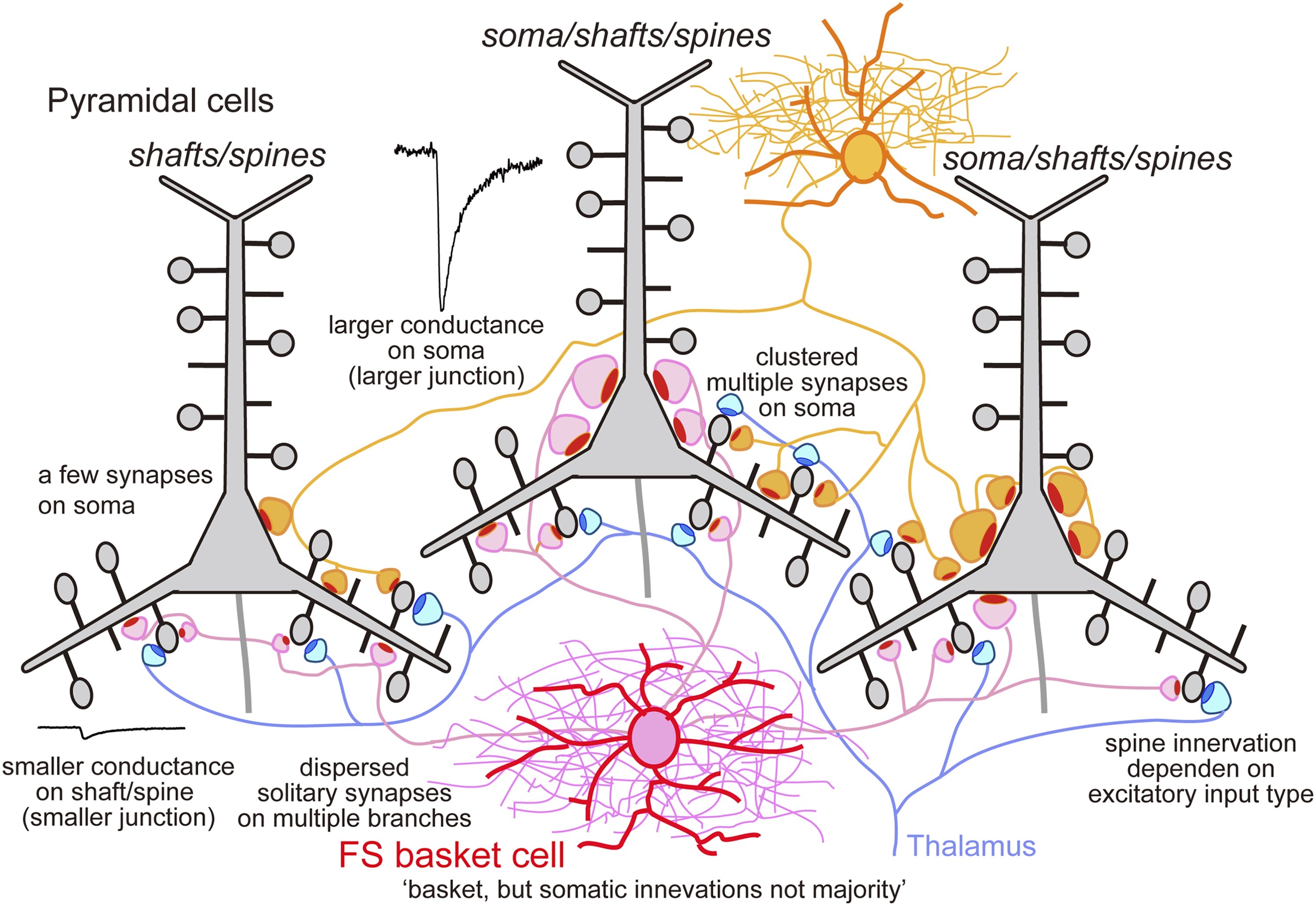
图17.5 大鼠大脑皮层第5层的锥体神经元既有来自自身更浅层的顶端树突汇总,又在接近细胞体的同层树突接受来自丘脑(兴奋性)和来自大篮状细胞(抑制性)的输入。来自[10]
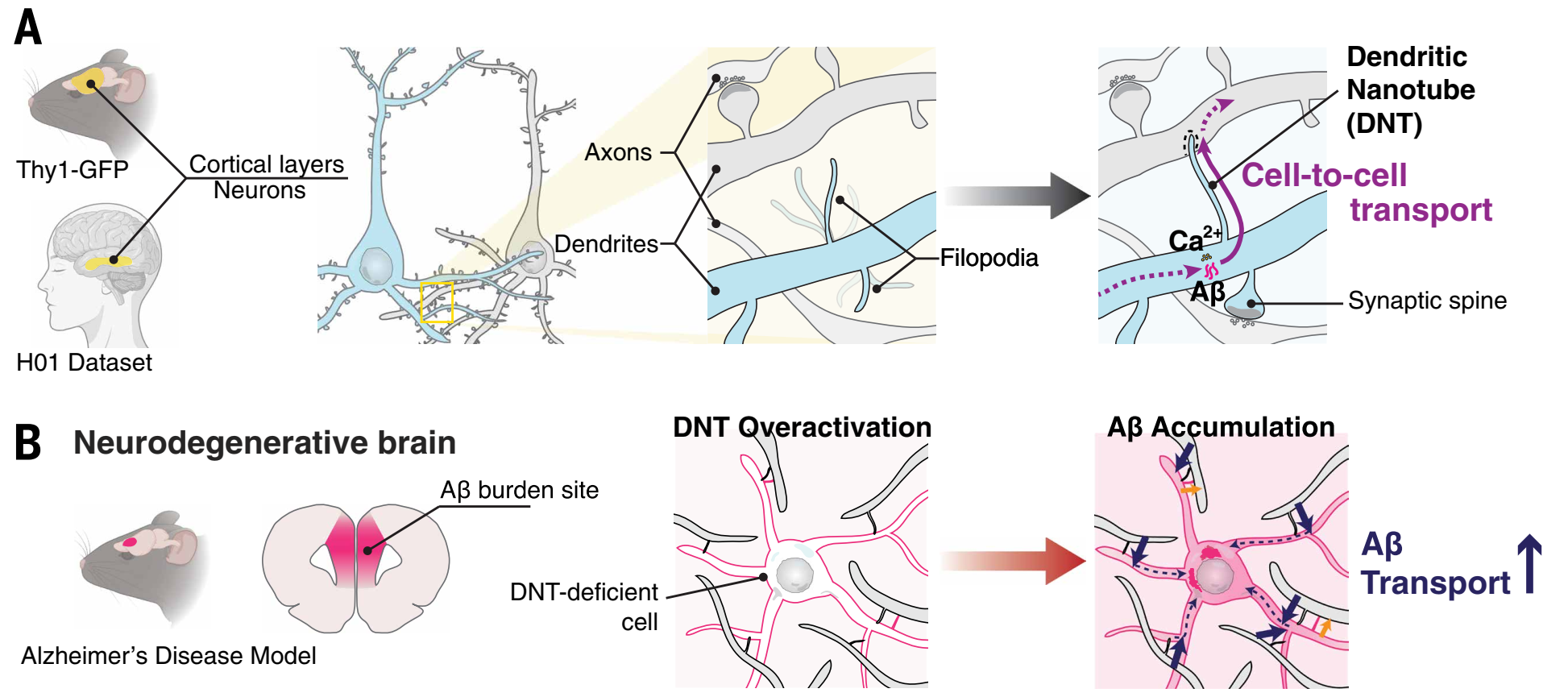
树突棘、突触扣节等神经元的亚细胞形态与构造为单个神经细胞的计算与存储以及在此基础上的神经网络性能提供了更多可能性,值得进一步探索。数亿年演化而来的亚细胞级信息分级管理,较好地兼顾了既有信息的存储与新经验的学习;局部的竞争性覆盖并不意味着信息的丢失,可能还可以在新刺激下重归主导。比如回家过个年,是不是又刷出了一些记忆?
[10] Kubota, Y. et al. Functional effects of distinct innervation styles of pyramidal cells by fast spiking cortical interneurons. Elife 4 (2015).
0
推荐




 京公网安备 11010502034662号
京公网安备 11010502034662号 