在讲快速眼动睡眠之前,我们先探讨一下脑电波在神经元及突触层面的物理基础。传统上,EEG脑电数据,按频率由慢到快以希腊字母从alpha开始命名,具体对应的频率在不同物种间存在差异,学界也有争议。小鼠的gamma波频率为30hz-150hz[1]。前面讲到,约200Hz的所谓尖波涟漪可能代表了锥体神经元突触的成簇放电(海马体的锥体神经元比大脑皮层的锥体神经元突触略大),而约100Hz的gamma波在睡眠(甚至白天走神或静息冥想)时常见,可能代表了大脑皮层表达小清蛋白的(大篮状细胞)中间神经元主导的活动[2]。 相比锥体神经元历时约~5ms的突触传递,中间神经元的突触传递过程往往需要10ms,可以解释gamma波比尖波涟漪慢的频率。大篮状细胞的电突触连接也使它们比锥体神经元更同步(较弱的电突触也可以不同步,图7.2)。
视觉导航是伴随着gamma和尖波涟漪频率产生的电信号而进行的[3, 4, 5, 6]。gamma波与theta波相位锁定(波峰波谷在时间上重叠)[7, 8]。人类大脑的theta波可以慢至1Hz(上限与小鼠等一样,大约10Hz)。
海马体、内嗅皮层等的theta波需要锥体神经元与几种抑制性的中间神经元共同作用(图21.1,图21.2)[9,10]。一项根据大鼠海马CA1区神经元组成的全尺寸数值模拟研究,包括了311,500个锥体神经元,27,240个多种类型的中间神经元(图21.2),以及454,700个对这些海马CA1神经元进行随机输入的神经元[10]。该模型成功再现了theta波,并得以分析各类中间神经元的贡献。虽然中间神经元总共占比不足10%,可以看到不同类型各自的放电特征与作用(图21.1)。大篮状细胞、小篮状细胞(cholecystokinin+ (CCK+) basket cells)、吊灯细胞等都与较低频的gamma波(这里25-80Hz)一致,但大篮状细胞以及其他一些中间神经元还与theta波一致[10]。这项模拟研究说明,不需要有节奏的外部输入,海马CA1多种神经元连接的固有特征即决定了theta波的产生和相位。
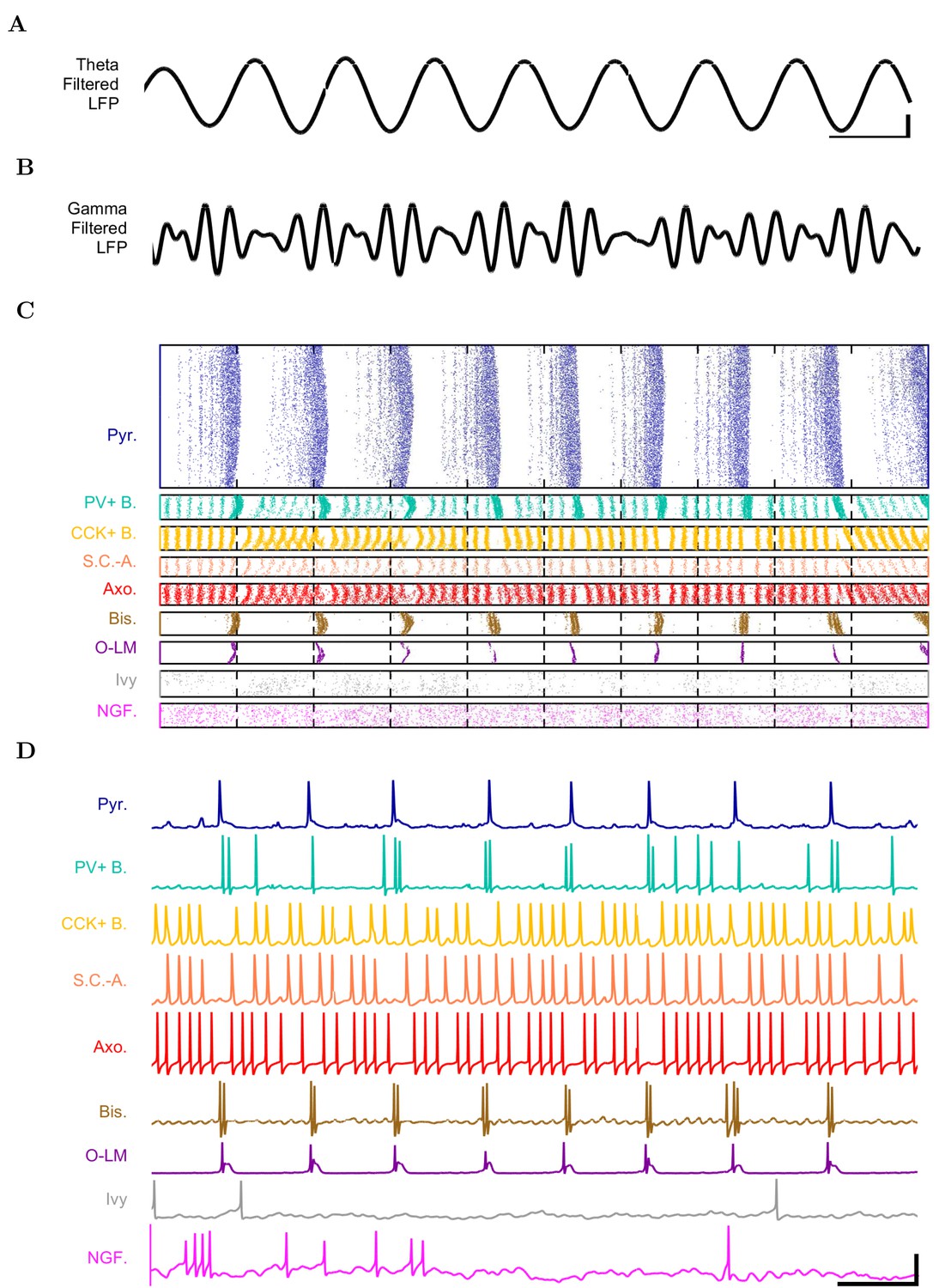
图21.1 对大鼠海马CA1各类神经元的完整模拟。Axo-axonic即枝形吊灯细胞。Bistratified是一类同时表达小清蛋白PV和生长抑素somatostatin的快速反应型中间神经元(小清蛋白对钙离子结合快)。Schaffer Collateral-Associated (SC-A) cells (CCK+, innervate dendrites in the stratum radiatum), oriens-lacunosum-moleculare (O-LM) cells (SOM+, project to the distal dendrites in the stratum lacunosum-moleculare, though their somata are located in the stratum oriens)。Ivy细胞与neurogliaform细胞较像,但作用于近端而不是远端树突。[10]
除了上述这些直接呈现振荡的锥体神经元和表达小清蛋白的中间神经元,海马neurogliaform中间神经元在上述模拟研究中对theta波的振荡强度(theta power, mV2^2/Hz)也是必须的[10]。这类早年被误认为像胶质细胞的中间神经元,树突较小,但轴突很密。
我们在本书第5节看到,大脑皮层第一层和第五层也有不少neurogliaform中间神经元。有研究表明,大脑皮层中neurogliaform中间神经元可以把锥体神经元从gamma震荡中解偶联[11],这也是一种决定性的调拨作用。
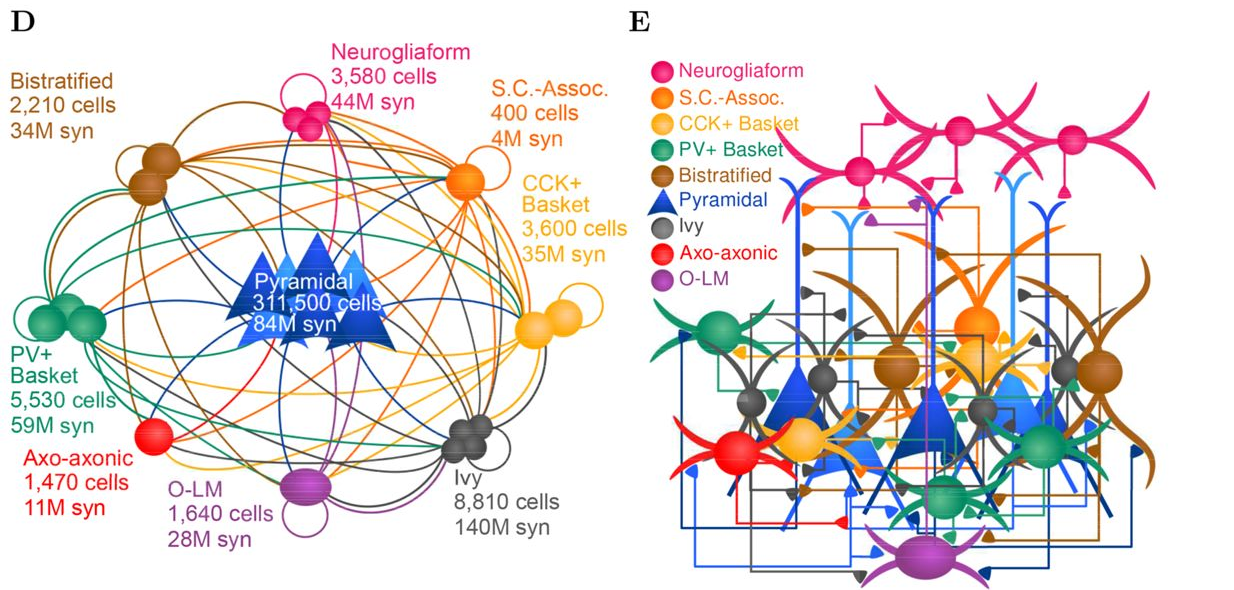
图21.2 对应图21.1大鼠海马CA1各类神经元模拟包括的具体神经元数目和突触数目。来自[10]
虽然图21.1的模拟显示外部输入不需要有节律,海马CA1就能产生节律,现实中theta经常受外部输入调控。一项只区分兴奋性神经元与抑制性神经元的模拟研究显示,当兴奋性外部电流输入较大时,theta波频率会增加,或者当抑制性突触具有较快的衰减时间常数时,theta波频率也会增加[12]。这么说来,人的theta波可以低至1赫兹,是更沉得住气的表现。
对不同频率的脑电波有了基于神经元及其突触的认识,我们下一节就可以讲做梦了。
参考文献:
[1] Adamantidis, Antoine R., Carolina Gutierrez Herrera, and Thomas C. Gent. 2019. “Oscillating Circuitries in the Sleeping Brain.” Nature Reviews Neuroscience 20 (12): 746–62. https://doi.org/10.1038/s41583-019-0223-4.
[2] Cardin, J. A., Carlén, M., Meletis, K., Knoblich, U., Zhang, F., Deisseroth, K., Tsai, L.-H., & Moore, C. I. (2009). Driving fast-spiking cells induces gamma rhythm and controls sensory responses. Nature, 459(7247), 663–667. https://doi.org/10.1038/nature08002
[3] Staudigl, T. et al. Hexadirectional modulation of high-frequency electrophysiological activity in the human anterior medial temporal lobe maps visual space. Curr. Biol. 28, 3325-3329.e4 (2018).
[4] Vaz, A. P., Inati, S. K., Brunel, N. & Zaghloul, K. A. Coupled ripple oscillations between the medial temporal lobe and neocortex retrieve human memory. Science 363, 975–978 (2019).
[5] Norman, Y. et al. Hippocampal sharp-wave ripples linked to visual episodic recollection in humans. Science 365 (2019).
[6] Abbaspoor S, Hussin AT, Hoffman KL. Theta- and gamma-band oscillatory uncoupling in the macaque hippocampus. Elife. 2023 May 4;12:e86548.
[7] Sirota, A. et al. Entrainment of neocortical neurons and gamma oscillations by the hippocampal theta rhythm. Neuron 60, 683–697 (2008).
[8] Tort, A. B. L., Scheffer-Teixeira, R., Souza, B. C., Draguhn, A. & Brankačk, J. Theta-associated high-frequency oscillations (110–160 Hz) in the hippocampus and neocortex. Prog. Neurobiol. 100, 1–14 (2013).
[9] Cobb, S. R., E. H. Buhl, K. Halasy, O. Paulsen, and P. Somogyi. 1995.“Synchronization of Neuronal Activity in Hippocampus by Individual GABAergic Interneurons.” Nature 378 (6552): 75–78. https://doi.org/10.1038/378075A0.
[10] Bezaire, M. J., Raikov, I., Burk, K., Vyas, D., & Soltesz, I. (2016). Interneuronal mechanisms of hippocampal theta oscillations in a full-scale model of the rodent CA1 circuit. ELife, 5. https://doi.org/10.7554/elife.18566
[11] Ece Sakalar, Klausberger, T., & Bálint Lasztóczi. (2022). Neurogliaform cells dynamically decouple neuronal synchrony between brain areas. Science, 377(6603), 324–328. https://doi.org/10.1126/science.abo3355
[12] Yang, Yihao, Howard Gritton, Martin Sarter, Sara J. Aton, Victoria Booth, and Michal Zochowski. 2021. “Theta-Gamma Coupling Emerges from Spatially Heterogeneous Cholinergic Neuromodulation.” PLoS Computational Biology 17 (7): e1009235. https://doi.org/10.1371/journal.pcbi.1009235.
0
推荐




 京公网安备 11010502034662号
京公网安备 11010502034662号 