我们前文提到过的位于小鼠或大鼠海马CA1区域的位置细胞(图25.1,图18.4,图22.1)与内侧内嗅皮层MEC的网格细胞共同确定位置(图27.1,图27.2,图27.3)。
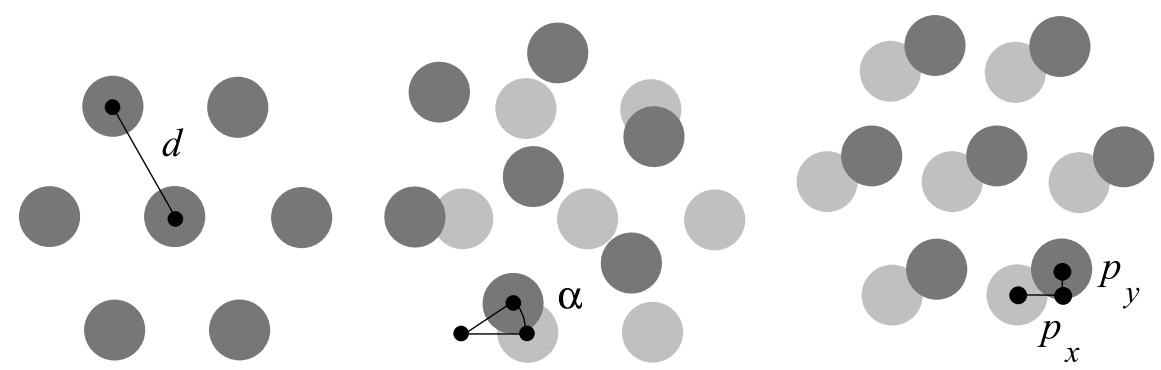
图27.1 网格细胞的网格间距d,朝向alpha和相位p三个基本参数。来自[1]。真实数据参考图26.1。
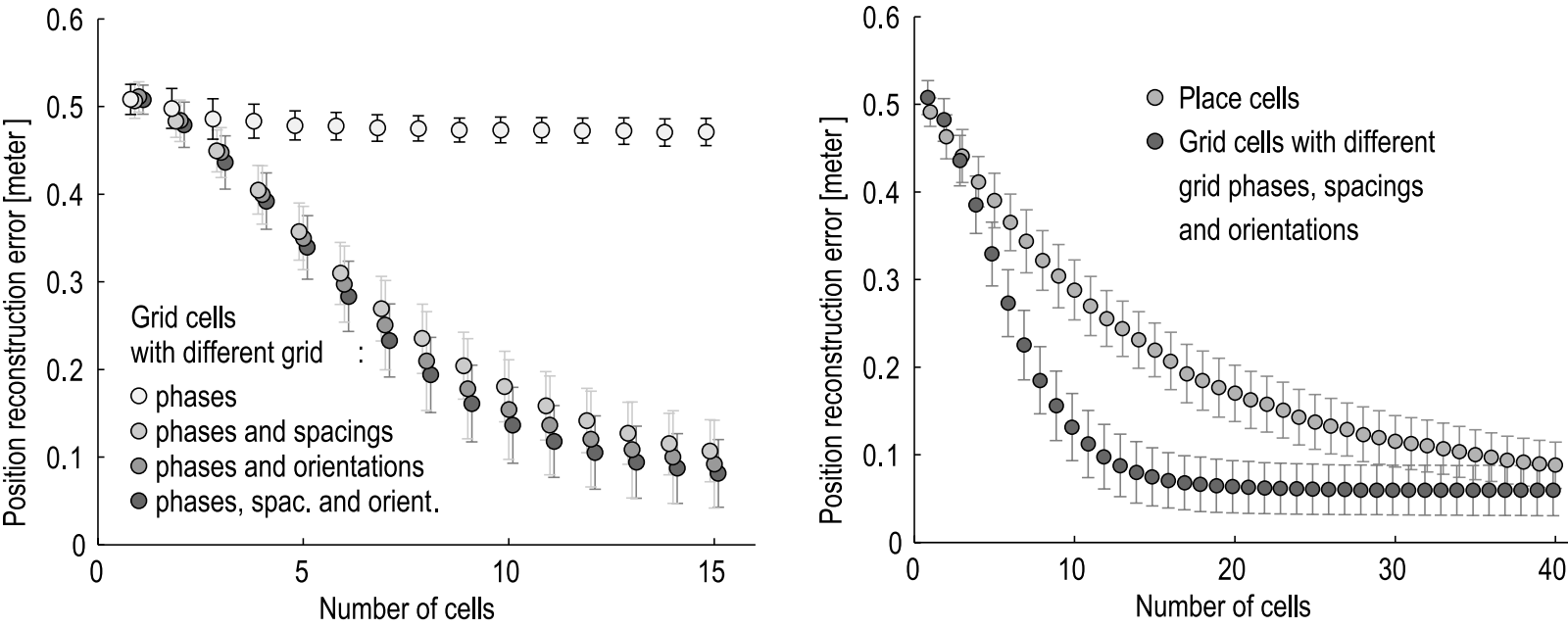
图27.2 网格细胞定位精度与参数。左图,网格细胞包括相位、间距、朝向参数后,定位错误随着细胞数目增加而降低。右图,位置细胞与网格细胞所需细胞数目比较。来自[2]。
位置细胞对应的海马CA1区域锥体神经元及其中间神经元可能有较大的树突、可以在不同阈值检测到信息(图18.4),多个连续的位置细胞还可以形成梯度,这些都可以解释位置细胞在本地比网格细胞更高的定位精度[2]。
另外,还有新研究报道了表征或凹或凸的转角的神经元[3],位于内嗅皮层折叠至海马前在中间过渡的下托(subiculum)区域(图27.3)。
类似位置细胞的吸引子(attractors)在人工智能研究中已多有应用(如[4,5])。但网格细胞可能是更节约细胞(图27.2右侧),而且更有逻辑框架的解决方案[4,6](本书后文继续),不必记住过多细节。从单个已知的位置外推,几步以后误差就明显累积。而不同大小的网格(第25节)可能是更适合新环境探索的。
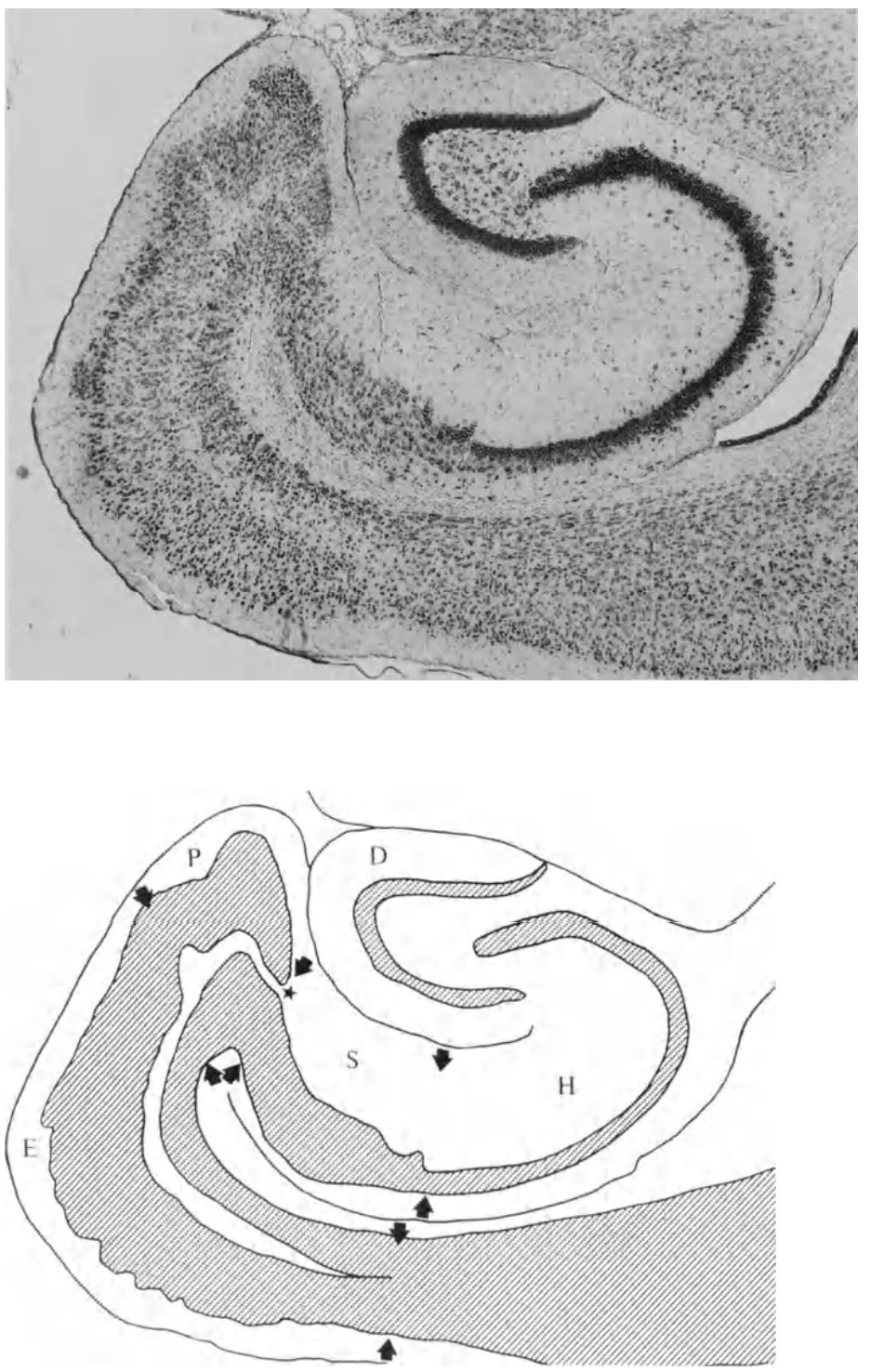
图27.3 大脑皮层(右侧更粗的灰色)内嗅皮层E至前下托P、下托S、海马体CA1-2-3(H)的折叠。齿状回D为独立层。小鼠俯视图。黑色为Nissl染色的神经元细胞核。前文已有。
在阿尔兹海默症患者中,tau 蛋白(一种可以聚集、对神经元有毒的蛋白质)聚集首先出现在内嗅皮层,随着时间的推移,海马体和大脑皮层(最先是第三层)也会受到影响[7]。携带阿尔茨海默病基因风险位点的年轻成年人(apoe-ε4等位基因)在功能磁共振成像(fMRI)已经表现出可检测到的网格状表征减少,以及对应的空间记忆能力受损[7]。另一方面,他们的海马体更加活跃,这可能被看成是一种对空间记忆受损的补偿[8]。这与有Apoe ε4等位基因的人有更好的视觉工作记忆相一致[9],年轻时可能博闻强记。网格细胞的空间表征与中间神经元、以及之后提到的头部方向细胞的放电同步化特征,在另一个阿尔兹海默症(过度表达淀粉样蛋白的转基因)小鼠模型中受到损害[10]。
而在重度抑郁障碍患者中,儿童时期身体或情感创伤史与内嗅皮层厚度呈负相关,而积极的个性特征则与海马、杏仁核的体积,以及楔前叶和扣带皮层的皮层厚度增加相关[11]。
在新物体-空间探索过程中,下丘脑的下视丘分泌素(hypocretin)神经元激活MEC中表达小清蛋白(PV)的中间神经元、促进伽马振荡。下丘脑下视丘分泌素神经元的这种对MEC的调控作用有助于增强空间记忆功能[12]。
上一节图26.3b展示了海马体与MEC之间的信息交换。海马CA1 的θ波(平均7 Hz;人类为2-10 Hz)与大脑皮层γ波的相位锁定(整倍关系),大约早50毫秒出现[13];参与恐惧记忆、强化学习等的前扣带皮层(ACC)还可以驱动下一轮MEC的θ波,进而驱动下一轮海马CA3、CA1区的 θ波[14,15,16,17,18,19],完成探索与生成的循环。这是我们后文会继续介绍的大脑中的迭代式生成对抗神经网络(Generative Adversarial Network)(图27.4)。内嗅皮层与海马体的组合,大致补齐了前文提到的海马体迭代更新的记忆哈希索引(图15.3)。
前文图21.1对海马CA1区theta波的模拟还没有考虑其他脑区。例如内嗅皮层MEC和LEC的抑制性中间神经元稀疏地作用于海马CA1的中间神经元,包括表达CCK的小篮状细胞,这预计可以增强同步性。MEC第Va层(图26.3b)的神经元还投射至前额叶皮层以及杏仁核,后者可能可以通过ACC再作用于海马。
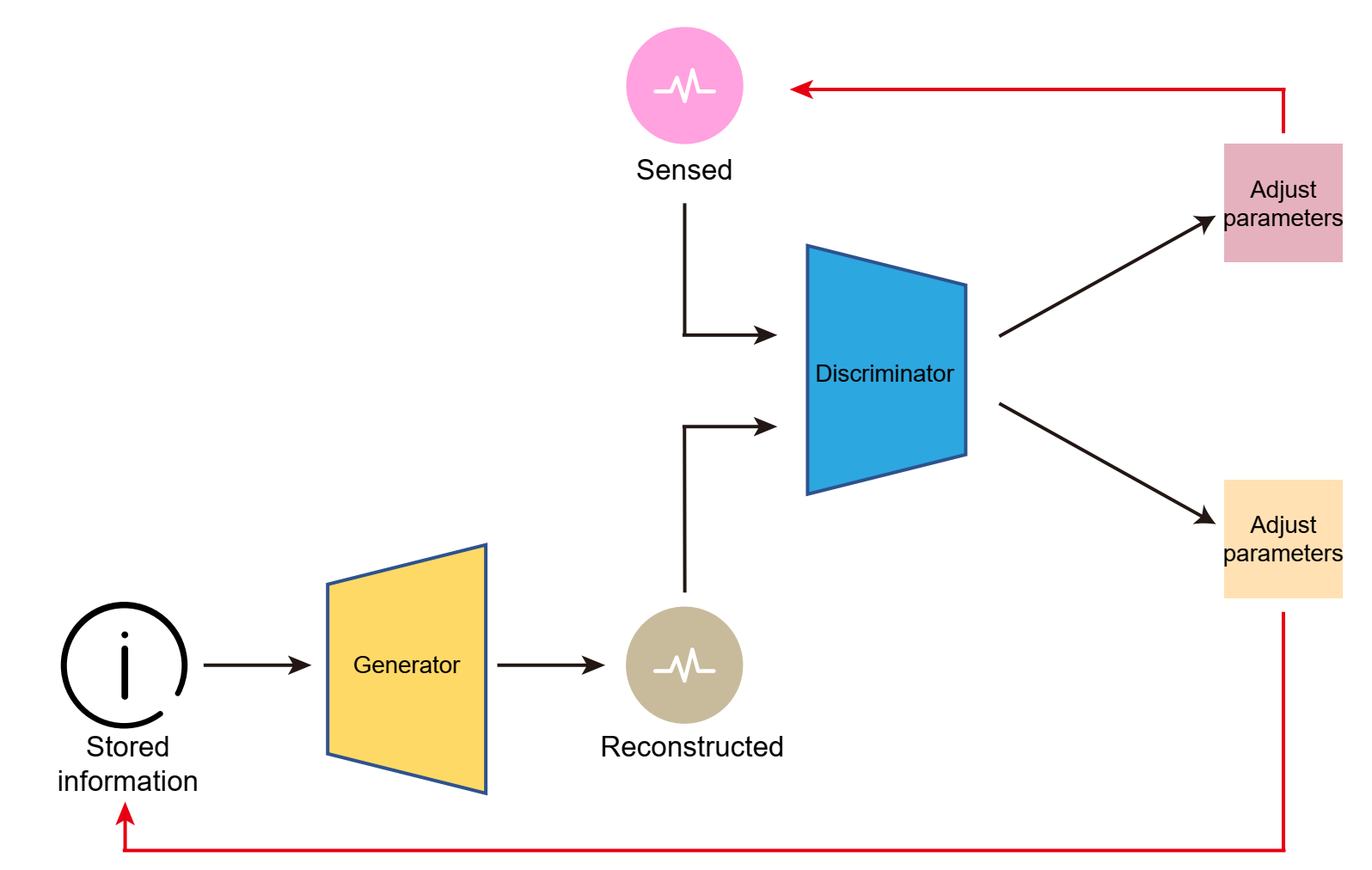
图27.4 大脑中离线与在线学习相结合的可迭代的生成对抗网络。来自大脑皮层的感官输入可以通过海马体的索引比较,有选择地更新在前额叶、运动皮层等的信息。MEC的网格作为降维、稀疏化的范式,更易调用与迁移学习,既可以快速调用海马体-大脑皮层的信息,自身的有向、有重点的网格又可以被迭代更新。后文还会介绍大脑皮层第6层成对的屏状核(claustrum)的“注意力”作用。在英文著作(https://www.jennystanford.com/9789814968782/
neuroscience-for-artificial-intelligence/)已有。
参考文献:
[1] Guanella, A., Kiper, D. & Verschure, P. A model of grid cells based on a twisted torus topology. Int. J. Neural Syst. 17, 231–40 (2007).
[2] Guanella, A. & Verschure, P. F. M. J. Prediction of the position of an animal based on populations of grid and place cells: a comparative simulation study. J. Integr. Neurosci. 6, 433–46 (2007).
[3] Sun Y, Nitz DA, Xu X, Giocomo LM. Subicular neurons encode concave and conves geometries. (2024) Nature. Mar;627(8005):821-829.
[4] Mulas M, Waniek N & Conradt J. Hebbian plasiticiy realigns grid cell activity with external sensory cues in continuous attractor models. (2016) Front Comput Neurosci. 10, 13.
[5] Stachenfeld, K. L., Botvinick, M. M. & Gershman, S. J. The hippocampus as a predictive map. Nat. Neurosci. 20, 1643–1653 (2017).
[6] Whittington, J. C. R. et al. The Tolman-Eichenbaum Machine: unifying space and relational memory through generalization in the hippocampal formation. Cell 183, 1249–1263.e23 (2020).
[7] Henstridge, Christopher M., Bradley T. Hyman, and Tara L. Spires-Jones. 2019. “Beyond the Neuron–Cellular Interactions Early in Alzheimer Disease Pathogenesis.” Nature Reviews Neuroscience 20 (2): 94–108.
[8] L, Kunz, Schröder TN, Lee H, Montag C, Lachmann B, Sariyska R, Reuter M, et al. 2015. “Reduced Grid-Cell-like Representations in Adults at Genetic Risk for Alzheimer’s Disease.” Science 350 (6259): 430–433. https://doi.org/10.1126/SCIENCE.AAC8128.
[9] Lu, Kirsty, Jennifer M. Nicholas, Yoni Pertzov, John Grogan, Masud Husain, Ivanna M. Pavisic, Sarah-Naomi James, et al. 2021. “Dissociable Effects of APOE Ε4 and β-Amyloid Pathology on Visual Working Memory.” Nature Aging, October. https://doi.org/10.1038/s43587-021-00117-4.
[10] Ying, Johnson, Alexandra T. Keinath, Raphael Lavoie, Erika Vigneault, Salah El Mestikawy, and Mark P. Brandon. 2022. “Disruption of the Grid Cell Network in a Mouse Model of Early Alzheimer’s Disease.” Nature Communications 13 (1): 886. https://doi.org/10.1038/s41467-022-28551-x.
[11] Yu, Meichen, Nicholas Cullen, Kristin A Linn, Desmond J Oathes, Darsol Seok, Philip A Cook, Romain Duprat, et al. 2021. “Structural Brain Measures Linked to Clinical Phenotypes in Major Depression Replicate across Clinical Centres.” Molecular Psychiatry 26 (7): 2764–75. https://doi.org/10.1038/s41380-021-01039-8.
[12] Liao, Y., Wen, R., Fu, S., Cheng, X., Ren, S., Lu, M., Qian, L., Luo, F., Wang, Y., Xiao, Q., Wang, X., Ye, H., Zhang, X., Jiang, C., Li, X., Li, S., Dang, R., Liu, Y., Kang, J., & Yao, Z. (2023). Spatial memory requires hypocretins to elevate medial entorhinal gamma oscillations. Neuron, 112(1), 155-173.e8.
[13] Sirota, A. et al. Entrainment of neocortical neurons and gamma oscillations by the hippocampal theta rhythm. Neuron 60, 683–97 (2008).
[14] Rueckemann, J. W., Sosa, M., Giocomo, L. M. & Buffalo, E. A. The grid code for ordered experience. Nat. Rev. Neurosci. 22, 637–649 (2021).
[15] Ray, S. et al. Grid-layout and theta-modulation of layer 2 pyramidal neurons in medial entorhinal cortex. Science 343, 891–896 (2014).
[16] Wang, T. et al. Modularization of grid cells constrained by the pyramidal patch lattice. iScience 24, 102301 (2021).
[17] Gu, Y. et al. A map-like micro-organization of grid cells in the medial entorhinal cortex. Cell 175, 736-750.e30 (2018).
[18] Hafting, T., Fyhn, M., Bonnevie, T., Moser, M.-B. & Moser, E. I. Hippocampus-independent phase precession in entorhinal grid cells. Nature 453, 1248–52 (2008).
[19] Zutshi, I., Valero, M., Fernández-Ruiz, A. & Buzsáki, G. Extrinsic control and intrinsic computation in the hippocampal CA1 circuit. Neuron 110, 658–673.e5 (2022).
0
推荐




 京公网安备 11010502034662号
京公网安备 11010502034662号 