空间导航系统,例如头部方向细胞,在动物第一次睁开眼睛之前就开始发育了。除了前文介绍的MEC的网格细胞、subiculum的凹凸面细胞、海马体的位置细胞,本节还会介绍其他头部方向细胞( head direction cells)、物体向量细胞(object vector cells)、速度细胞等其他一些有助于动物准确感知空间和时间的细胞。
大鼠有专门负责感受自己接近了边界的边界向量细胞,有边界在前面的,也有感受背后的(图28.1)[1]。这与自动驾驶等应用的逻辑是一致的。除了空间感知,在后文的社交等领域可能也有类似的细胞。
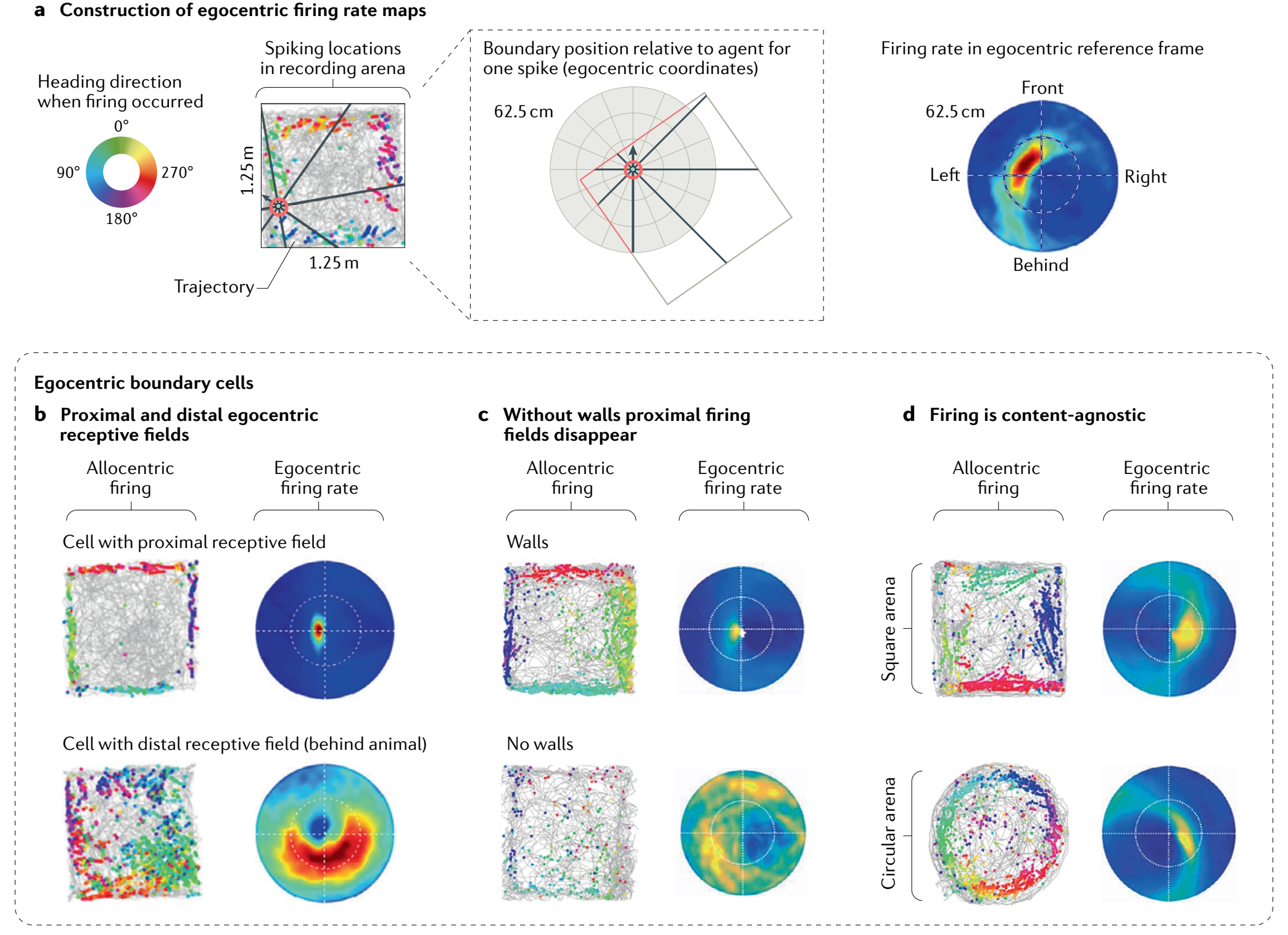
图28.1 以自我中心的向量编码细胞。(a)自我中心编码的一个例子。正方形场地中的灰线显示大鼠或小鼠所走的轨迹。彩色的点根据头部朝向着色,图中的点为在纹状体中的一个自我中心边界细胞的放电位置。红色圆圈和黑色箭头显示了动物在该边界细胞放电时的位置和朝向。中间子图显示了在发射这个尖峰时,相对于动物的边界位置(红线),以动物为中心的参考系中绘制的边界位置。右图为该细胞在以自我为中心的参照系中坐的放电率图,暖色的更强。(b)两种位于纹状体的自我中心边界细胞的例子。上图为一个感受接近边界的细胞。下图为一个感受背后有边界的细胞,感受野较大。(c)一个位于压后(retrosplenial)皮层的细胞具有近端感受野,在移除边界后不再放电。(d)压后皮层自我中心边界细胞放电不受边界或方或圆的形状影响。来自[1]。
无论是以自我为中心(egocentric)还是以外物为中心(allocentric)放置参照系,除了海马体的位置细胞和内侧内嗅皮层的网格细胞,海马体及其周边还有一些比如头部方向细胞,对于空间尤其是方向的感知很重要。比如鹌鹑的海马结构(hippocampal formation,还包括下托、内嗅皮层)可以检测到表征头部朝向的细胞(图28.2)[2]。与我们在视觉、记忆、时间等看到的一样,大部分细胞可能只是略有调制。当作为头部朝向线索的光源旋转了180度以后,大部分细胞没有这么大的变化,只有一小部分的反应也转了180度(图28.2)[2]。
大鼠等的研究也表明,在出现较大的朝向误差后,头部方向细胞会进行“重新校准”,确定新的方向[3]。
小鼠丘脑的头部方向细胞在播放声音和触摸小鼠鼻子上的触须时,被特异性地、可靠地激活,而且延迟时间极短。这打破了之前认为头部方向细胞不受感官刺激的传统认知[4],但与丘脑接受小脑输入、进一步处理感官信息给大脑皮层的功能一致,我们在睡眠章节也看到了丘脑的作用。
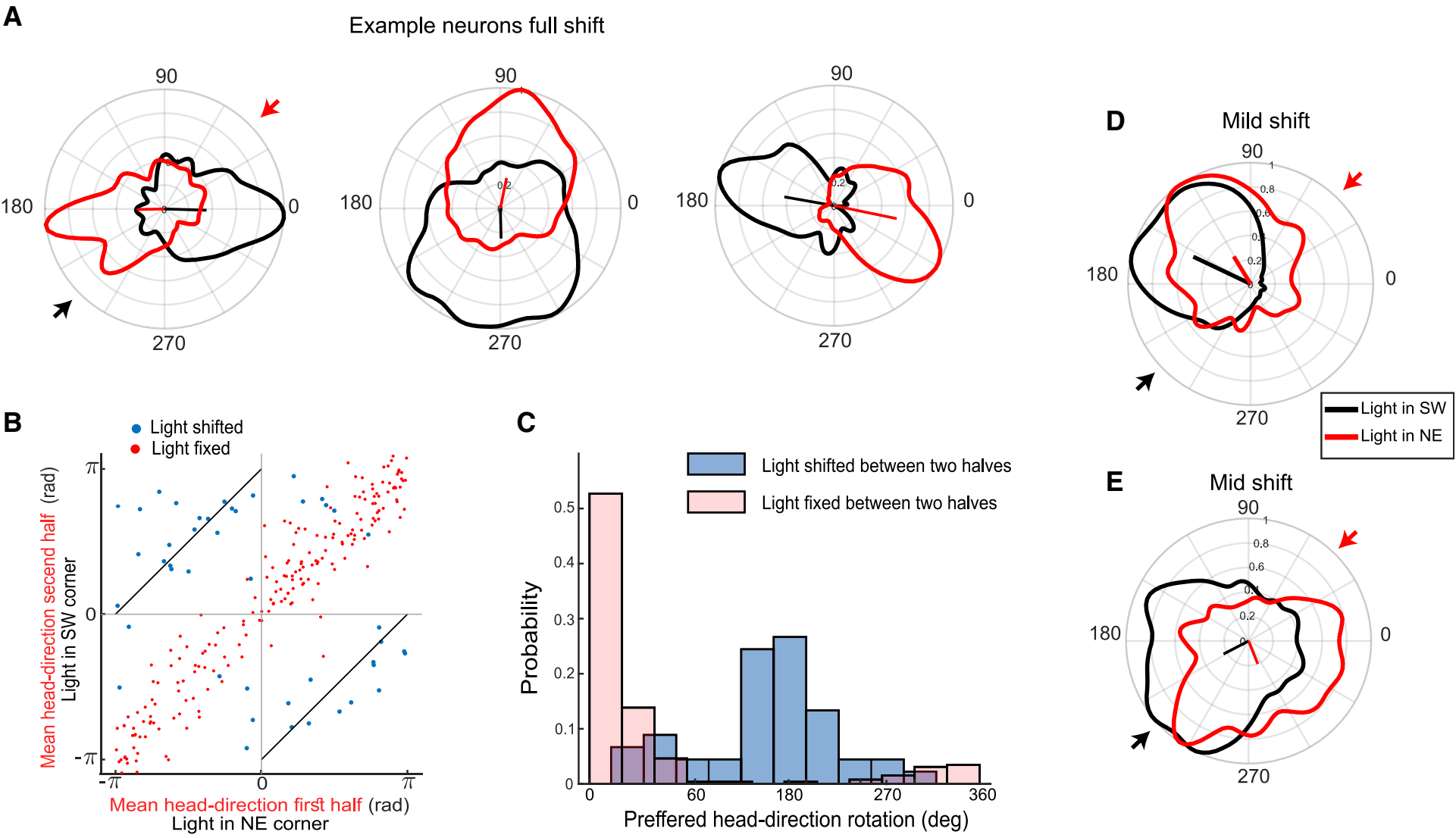
图28.2 鹌鹑海马头部方向(HD)细胞对线索旋转的反应。鹌鹑(Coturnix japonica)戴着植入的细胞外检测自由探索1×1平方米的开放场地。(A)在180°线索旋转(光源移动)前后,三个响应也转180度的细胞的头部方向调谐曲线示例。曲线的红或黑色与圈外箭头标注的光源位置一致,中心出发的Rayleigh向量颜色也一致。(B)将第二段时间内的首选头部方向与第一段时间内的首选头部方向绘制在一起。蓝色点表示在半程时将光源移动180°的结果。作为比较,用红色叠加了图3D中的点,以显示无线索移动的结果。黑色对角线表示首选方向的预测180°移动。(C)当光源移动180°(蓝色)与不移动(粉色)时,测量的两半时间段内首选头部方向差异的分布。(D)一个在光源旋转180°后旋转较小的细胞的例子。(E)一个响应中等的神经元的例子,其调谐方向大约是预测移动的一半。来自[2]。
我们前文还提到海马体有表征故事线的作用。大鼠研究中,位于丘脑前背侧核(anterior dorsal nucleus (ADN))的头部朝向随着远端标志物转动,而海马CA1的位置细胞对近端原有线索与旋转了的远端标志物都有表征(图28.3)[5]。这体现了不同类型细胞组合可以实现的更复杂的功能。说不定什么时候又转回去了。
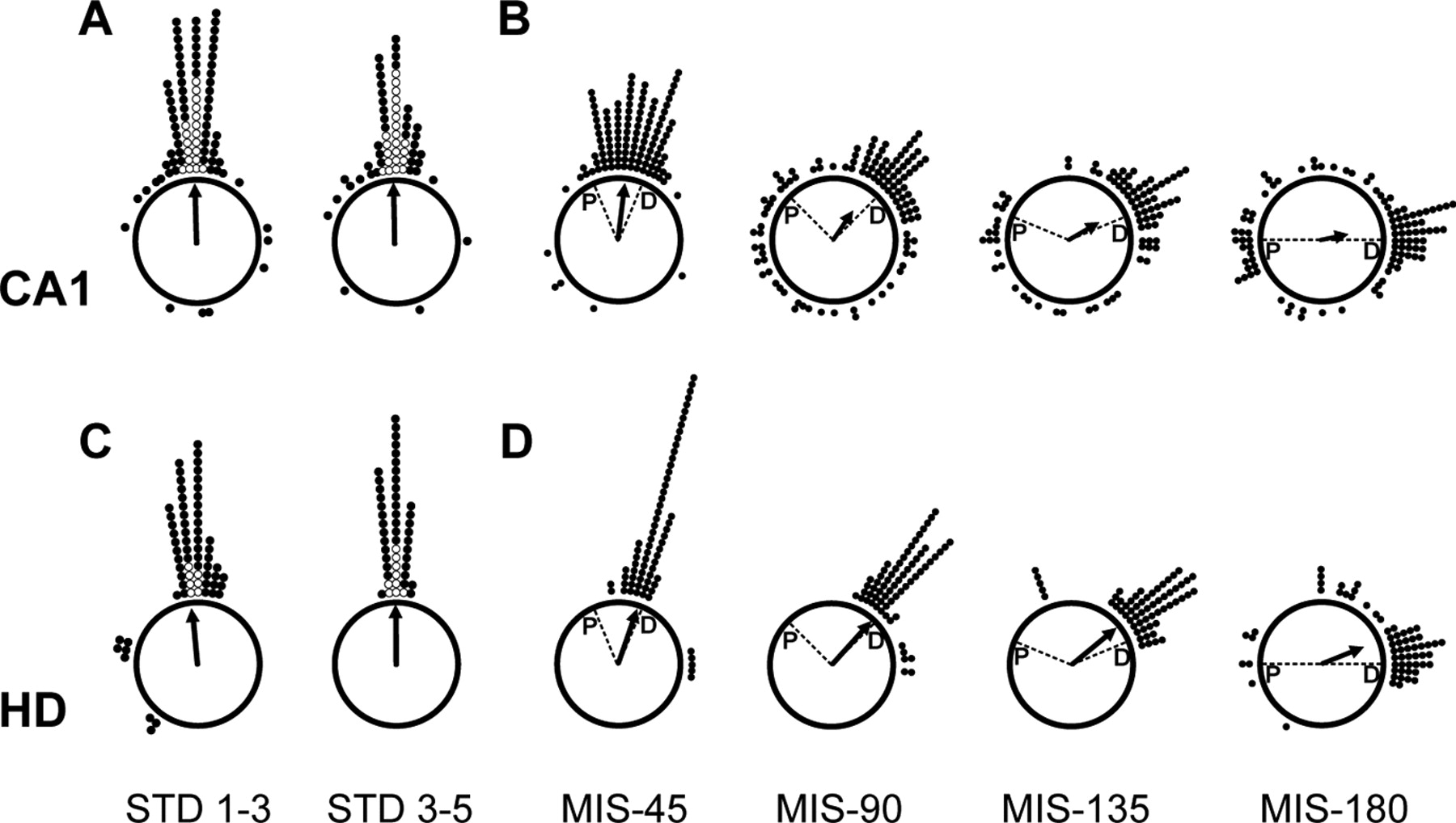
图28.3 大鼠丘脑ADN的头部朝向细胞与海马CA1位置细胞对比的极坐标图(polar plot)。STD为线索一致的情形,MIS为远端(D)旋转、相对近端(P)错配的情形。空心点代表10个数据点,实心点代表1个数据点。来自[4]
内耳的三个相互正交的半圆形的前庭半规管直接感受着我们在三维空间中的运动。与听觉类似,机械扰动通过内耳的毛细胞形成电信号以感知自身运动。经过一些训练,坐在旋转平台上的猴子的小脑核的神经元学会了在旋转时不激活,然后在旋转停止时再次激活(图28.4)[6]。这些猴子也许像我们一样,在旋转椅停止时感到头晕。
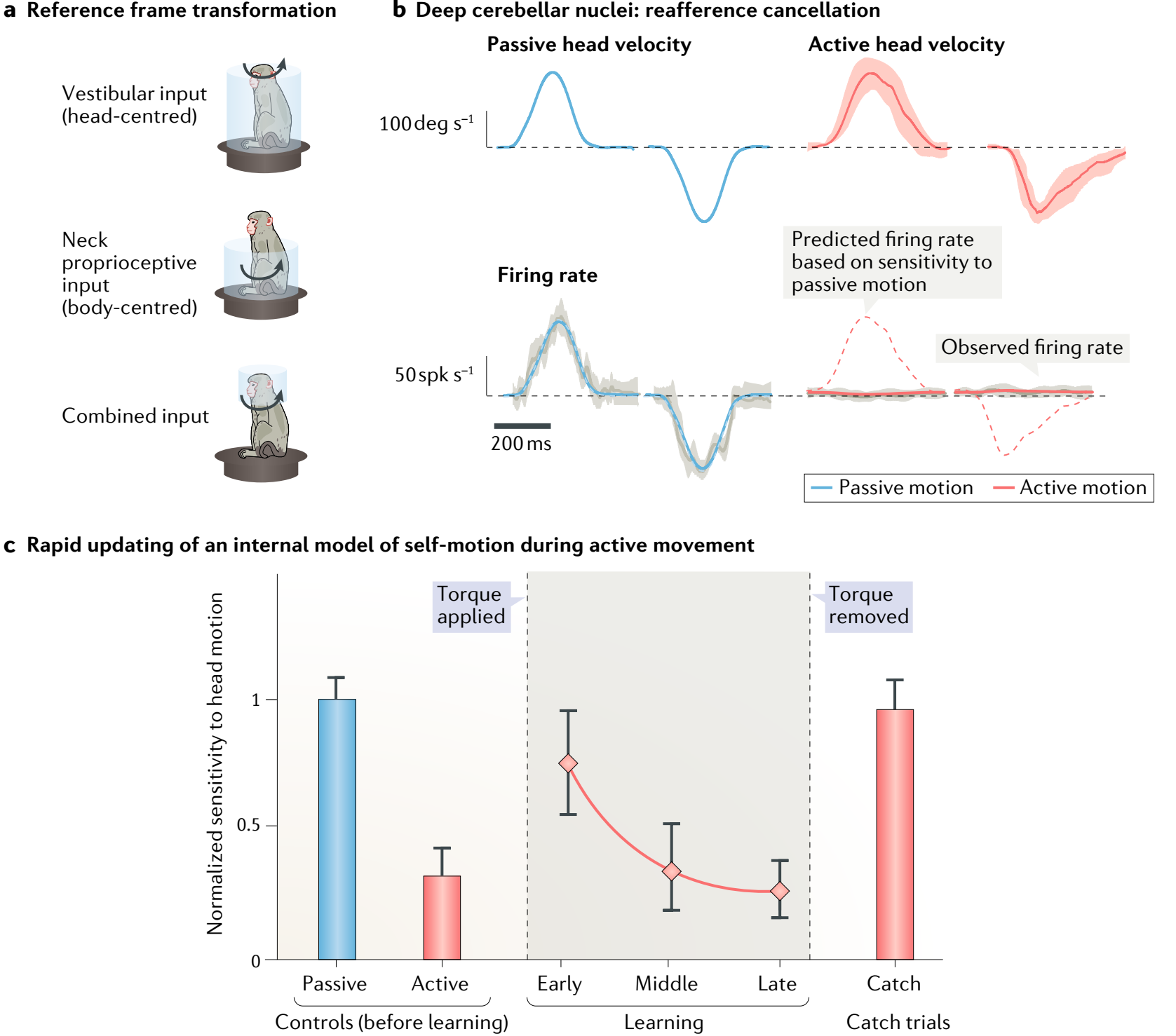
图28.4 内耳小脑模型中的自我运动模型。(a) 示意图展示了恒河猴的平衡感(头中心)和本体感知(身体中心)系统的刺激。平衡感系统通过将头部和身体一起相对于空间旋转(整体旋转;顶部子图)来刺激,而本体感觉系统通过将头部保持在静止状态,仅将身体旋转来刺激(中间子图)。相比之下,将头部相对于身体旋转(底部子图)会产生平衡感和本体感觉系统的联合刺激,从而允许我们研究从头中心坐标到身体中心坐标的平衡感输入的转换。(b) 在被动和主动(自愿)运动范式中,一个小脑核神经元深处的响应。顶部轨迹展示了头部速度,底部轨迹显示了神经元的放电率响应,虚线红线表示基于神经元对被动运动的敏感性预测的放电率在主动条件下。神经元在受到被动运动刺激时表现出强烈的调制,但当相同的运动被主动产生时,其响应最小。在底部子图中,灰色阴影对应于同一次运动的平均放电率和标准差。叠加的蓝色和红色线分别显示了被动和主动运动条件下的平均放电率响应。(c) 当通过施加阻力负载(扭矩)改变头部运动命令和结果运动之间的关系时,在主动头部运动期间,神经元对头部运动的平衡觉敏感性最初增加到被动头部运动期间测量的水平。然后逐渐降低到在施加扭矩之前主动头部运动期间测量的水平。一旦大脑的内部模型被更新以适应自愿头部运动命令和结果运动之间的新关系,在旋转被移除的主动试验中,神经元的敏感性与被动头部运动期间的神经元敏感性相当。值得注意的是,学习过程中传入抑制的重新出现,表现为神经元响应的敏感性正常化程度的降低,与头部运动误差(未显示)的相应变化遵循相同的时间过程。来自[6]
很多人都会对速度或者加速感到兴奋。对速度的感知可能生死攸关。从脑干的脚桥被盖核(pedunculopontine tegmental nucleus)、Broca斜带的水平支,再到内侧内嗅皮层MEC,都有神经元在速度增加时放电增加,也有神经元在速度增加时放电减少[7, 8]。这样双向的刻画,预计是更准确的调制。抑制表达小清蛋白的抑制性中间神经元(对应于大篮状细胞或枝形吊灯细胞)会损害对自身速度的速度感知[9,10],提示这些中间神经元与速度感知有关。我们在时间的章节还看到了海马体中神经元对速度的表征(图24.1)。
伴随MEC的速度细胞,海马体还通过加速度信息来与之互补。海马体θ波频率(与兴奋性电流输入成正比)受跑步大鼠加速度的控制,进一步增加了导航的准确性[11]。有趣的是,对于患有2型糖尿病或阿尔茨海默病的前期的人群,推荐进行高强度间歇训练(HIIT)而不是慢跑[12, 13],这可能也与刺激加速度相关脑区有关。
我们对空间感知的理解可能还并不完整,但这不妨碍在自动化等方向的实践中进一步完善。我们在本书最后会看到,这一套基础的空间探索系统可能被用于包括因果推断在内的目前人工智能尚不擅长的功能。
参考文献:
[1] Bicanski, A. & Burgess, N. Neuronal vector coding in spatial cognition. Nat. Rev. Neurosci. 21, 453–470 (2020).
[2] Ben-Yishay, E. et al. Directional tuning in the hippocampal formation of birds. Curr. Biol. 31, 2592–2602.e4 (2021).
[3] Valerio S. & Taube J. S. Path integration: how the head direction signal maintains and corrects spatial orientation. Nat. Neurosci. 15, 1445–1453 (2012).
[4] Blanco-Hernández, E., Balsamo, G., Preston-Ferrer, P. et al. Sensory and behavioral modulation of thalamic head-direction cells. Nat Neurosci 27, 28–33 (2024).
[5] Yoganarasimha, D., Yu, X. & Knierim, J. J. Head direction cell representations maintain internal coherence during conflicting proximal and distal cue rotations: comparison with hippocampal place cells. J. Neurosci. 26, 622–31 (2006).
[6] Cullen, Kathleen E. 2019. “Vestibular Processing during Natural Self-Motion: Implications for Perception and Action.” Nature Reviews Neuroscience 20 (6): 346–63. https://doi.org/10.1038/s41583-019-0153-1.
[7] Carvalho, Miguel M, Nouk Tanke, Emilio Kropff, Menno P Witter, May-Britt Moser, and Edvard I Moser. 2020. “A Brainstem Locomotor Circuit Drives the Activity of Speed Cells in the Medial Entorhinal Cortex.” Cell Reports 32 (10): 108123.
[8] Dannenberg, Holger, Hallie Lazaro, Pranav Nambiar, Alec Hoyland, and Michael E. Hasselmo. 2020. “Effects of Visual Inputs on Neural Dynamics for Coding of Location and Running Speed in Medial Entorhinal Cortex.” ELife 9: 1–34. https://doi.org/10.7554/ELIFE.62500.
[9] Markram, H. et al. Interneurons of the neocortical inhibitory system. Nat. Rev. Neurosci. 5, 793–807 (2004).
[10] Yang, Y. et al. Theta-gamma coupling emerges from spatially heterogeneous cholinergic neuromodulation. PLoS Comput. Biol. 17, e1009235 (2021).
[11] Kropff, E., Carmichael, J. E., Moser, E. I. & Moser, M.-B. Frequency of theta rhythm is controlled by acceleration, but not speed, in running rats. Neuron 109, 1029–1039.e8 (2021).
[12] Silva, Djeniffer Elias da, Antônio José Grande, Leonardo Roever, Gary Tse, Tong Liu, Giuseppe Biondi-Zoccai, and Joni Márcio de Farias. 2019. “High-Intensity Interval Training in Patients with Type 2 Diabetes Mellitus: A Systematic Review.” Current Atherosclerosis Reports 21 (2): 8.
[13] Jensen, Camilla Steen, Justyna Maria Bahl, Lærke Borg Østergaard, Peter Høgh, Lene Wermuth, Amanda Heslegrave, Henrik Zetterberg, Niels H H Heegaard, Steen Gregers Hasselbalch, and Anja Hviid Simonsen. 2019. “Exercise as a Potential Modulator of Inflammation in Patients with Alzheimer’s Disease Measured in Cerebrospinal Fluid and Plasma.” Experimental Gerontology 121: 91–98.
0
推荐




 京公网安备 11010502034662号
京公网安备 11010502034662号 